서 론
Gitelman 증후군은 1966년 Gitelman 등[1]에 의해 처음으로 기술된 가족성의 저칼륨혈증, 저마그네슘혈증, 대사성 알칼리증, 저칼슘뇨증을 나타내는 증후군으로 과거 한때 Bartter 증후군으로 오인 또는 이의 변형으로 생각되었으나[2-4] 최근 분자 유전학의 발달에 의해 병태생리가 밝혀짐에 따라 Bartter 증후군은 Henle 고리비후 상행각에서의 염소 재흡수의 장애로 인한 저혈량증에 의해 유발되며 Gitelman 증후군은 원위곡 세뇨관의 Na-Cl cotransporter의 장애 때문임이 알려졌다[5].
국내에서는 Park 등[6]이 1996년 65세 여자에서 발생한 Gitelman 증후군 1예를 보고하였고 Kim 등[7]이 2002년 신장청소검사를 이용하여 진단한 Gitelman 증후군 2예를 보고한 바 있으며, 소아 연령에서는 Moon 등[8]이 2000년 소아과 추계학술대회에서 2예를 발표하였으나 아직 비교적 드문 질환으로 생각된다. 저자들은 손발 저림을 주소로 내원하여 저칼륨혈증, 대사성알칼리증, 저마그네슘혈증, 저칼슘뇨증 및 요중 칼슘과 크레아티닌의 비율이 0.2 이하를 보여 Gitelman 증후군으로 진단된 1예를 경험하였기에 문헌고찰과 함께 보고하는 바이다.
증 례
12세의 여자 환아가 내원 1일 전 저녁부터 흉부 불쾌감, 손발 저림증상을 보여 순천향대학교 천안병원 응급실에 내원할 당시 체온이 38°C였으며 혈액검사에서 저칼륨혈증소견을 보였다. 또한, 2007년 당시 발열, 기침으로 순천향대학교 천안병원 응급실 방문, 원인 불명의 저칼륨혈증 진단을 받았던 과거력이 있었으나 이후 특별한 치료를 받지 않고 지냈고 평소에도 1년에 1-2회 정도 간헐적으로 손이 뒤틀리는 양상의 근경축증상이 있었다. 이뇨제나 하제 등 약물을 복용한 적은 없었고 가족력도 특이한 사항이 없었다.
입원 당시 혈압은 110/70 mm Hg, 맥박 80 회/분, 호흡수 18 회/분, 체온은 38°C였다. 신장 165 cm, 체중 65 kg이었고 의식은 명료하였으며 결막은 창백하지 않았고 공막에 황달은 없었다. 경부 진찰 시 경정맥 확장은 보이지 않았고 촉진되는 림프절은 없었으며, 흉부 진찰에서 호흡음은 청명하였고 심음은 규칙적이며 심잡음은 들리지 않았다. 복부 진찰 시 특이소견은 없었고 하지의 함요 부종은 없었으며 감각은 정상이었으나 운동은 양쪽 상지 모두 움직일 수 있고, 근육 수축도 있으나 저항은 이기지 못하는 grade 4로 체크되었고 Trousseau’s sign 및 Chvostek’s sign은 음성이었다.
또한 혈청 전해질검사에서 Na 143 mEq/L, K 2.8 mEq/L, Cl 93 mEq/L로 저칼륨혈증소견을 보였고, 정맥혈가스분석에서 pH 7.469, PaCO2 51.1 mm Hg, PaO2 20.8 mm Hg, HCO3- 33.1 mEq/L로 대사성 알칼리혈증을 나타냈다. 혈청 삼투질 농도 293 mOsm/kg, 요 삼투질 농도 409 mOsm/kg, 일회뇨(spot urine)검사에서 Na 30.8 mEq/L, K 15.2 mEq/L, Cl 39.8 mEq/L, Ca 0.1 mg/dL, creatinine (Cr) 37.5 mg/dL이었다. 24시간 요 칼슘 배설양은 7.6 mg, 공복상태에서 측정한 일회뇨의 Ca/Cr 농도 비(mg/mg)는 0.002로 저칼슘뇨증을 보였다. 혈청 생화학검사에서 albumin 5.1 g/dL, Ca 8.7 mg/dL, P 4.8 mg/dL, blood urea nitrogen 11.1 mg/dL, Cr 0.4 mg/dL, uric acid 5.7 mg/dL, Mg 1.4 mg/dL (순천향대학교 천안병원 검사실 정상치 1.9-2.9)로 저마그네슘혈증을 보였다. 혈장 rennin 활성도는 17.13 ng/mL/hr (앙와위 시 정상치 0.68-1.36, 기립 시 정상치 0.24-4.70 ng/mL/hr), aldosterone 63.16 pg/mL (성인 앙와위 시 정상치 10-105, 성인 기립 시 정상치 34-273 pg/mL)이었으며 갑상선호르몬 및 부갑상선호르몬은 정상이었다. 흉부 방사선촬영과 뇌 자기공명영상촬영에서 특이소견은 없었다.
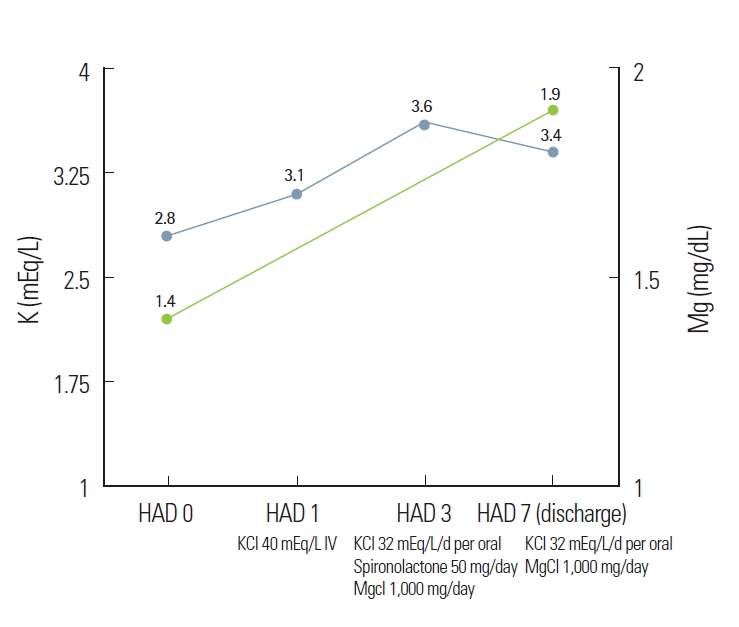
제1병일째 염화칼륨 40 mEq/L로 IV투여한 후 측정한 혈청 칼륨 농도는 2.8 mEq/L에서 3.1 mEq/L로 상승을 보였고, 제3병일째 염화칼륨 경구 투여로 32 mEq/day, spironolactone 50 mg/day, 염화마그네슘 1,000 mg/day를 복용 후 혈청 칼륨농도는 3.6 mEq/L로 상승하고 제5병일째 손발 저림증상은 호전을 보였으며 고알도스테론증 소견은 없어 spironolactone 복용을 중단하였다. 제7병일째 염화칼륨을 경구 투여하고(32 mEq/day), 염화마그네슘 1,000 mg/day 복용을 유지하면서 퇴원하였으며, 현재 혈청 칼륨 농도는 3.4 mEq/L, 마그네슘 농도는 1.9 mg/dL로 유지되고 있고, 오심 및 상지근 경축 등의 증상 없이 외래 추적 관찰 중이다(Fig. 1).
고 찰
Gitelman 증후군은 Gitelman 등[1]이 3예의 성인 환자를 처음 보고한 것으로 저칼륨혈증, 대사성알칼리증, 저마그네슘혈증 등을 보이는 질환이다. 이후 많은 환자들이 보고되었으며, Bartter증후군으로 기술된 환자에서도 실제로는 Gitelman 증후군이 많을 것으로 사료된다. 비교적 최근까지 Gitelman 증후군이 Bartter 증후군으로 잘못 진단되거나, Bartter 증후군의 한 아형으로 간주되어 왔기 때문이고[2-4], 현재는 Bartter 증후군과는 다른 새로운 증후군으로 받아들여지고 있다[9,10]. 실제로 Bartter 증후군으로 진단되었던 34명의 소아 환자들을 후향적으로 다시 검사해 본 결과 그 중 16명이 Gitelman 증후군을 가지고 있었다는 보고가 있다[9].
Bettinelli 등[9]은 Gitelman 증후군을 Bartter 증후군과 구별하는 기준을 제시하였는데 첫째, 현저한 저칼슘뇨증(요중 칼슘 <2 mg/kg/day; 정상치 >4 mg/kg/day) 및 요중 칼슘과 크레아티닌의 비율(urinary Ca/Cr ratio)이 0.2 이하이고 둘째, 저마그네슘혈증(혈청 마그네슘 <0.5 mEq/L; 정상치 0.8-1.0 mEq/L)이며, 셋째, 8세 이후 증상이 발현된다는 것이다[9].
본 환자는 손발 저림증상으로 내원하여 혈액검사에서 저칼륨혈증이 발견되었고 그 후 시행한 혈액검사 및 24시간 요검사에서 요중 칼슘 배설이 낮고 요중 칼슘과 크레아티닌의 비율이 0.2보다 낮으며 저마그네슘혈증이 보여 Gitelman 증후군으로 진단되었다.
Bartter 증후군은 Henle 고리의 상행각에서 염소의 재흡수의 장애로 인해 초래된다고 알려져 있으며 신장으로의 칼륨 유실에 의한 저칼륨혈증, 대사성 알칼리혈증, 고혈압을 동반하지 않는 혈장 레닌과 알도스테론의 상승은 Gitelman 증후군과 같은 양상을 보인다. 그러므로 Gitelman 증후군을 진단하기 위해서는 Bartter 증후군, 장기간의 이뇨제 사용, 마그네슘 결핍, 구토, 설사 및 하제 복용 등을 반드시 감별하여야 한다. 본 증례에서는 환자가 이뇨제 사용 및 하제 복용들의 약물복용력이 전혀 없었기 때문에 이뇨제 부하검사를 시행하지 않았다.
Gitelman 증후군은 상염색체 열성 유전을 하고, 1996년 Simon 등[11]에 의해 원인이 16q13에 있는 SLC12A3의 불활성화로 Na-Cl cotransporter에 결함이라는 사실이 밝혀졌다. 그러나 본 증례에서는 가족들의 혈액검사나 유전자검사를 시행하지 못해 아쉬운 점으로 남는다.
증상은 대부분 무증상이며 일시적인 피로나 근무력감, 테타니증상을 나타내기도 하고 때때로 복통, 구토, 열 등을 보이기도 하며 주로 성인에서 발견된다. 또한 국내에서 Park 등[12]이 2004년 11세 여자에서 간질 발작으로 내원하여 생화학적 검사 및 유전자검사에서 Gitelman 증후군으로 확진된 1예를 보고하였다. 본 환자의 경우, 손발 저림, 내원 당시 열, 흉부 불쾌감 등을 호소하였다. 생화학적 검사에서 저칼륨혈증, 저마그네슘혈증, 대사성알칼리증, 저칼슘뇨증이 관찰되며, 고레닌 고알도스테론혈증이 있어 Bartter 증후군과 혼동되기 쉽다.
치료는 저칼륨혈증 및 저마그네슘혈증에 의한 증상을 경감시키는 데 주안점을 둔다. 대부분의 경우 마그네슘염의 투여만으로 충분하며 칼륨염이나 프로스타글란딘 억제제는 필요하지 않다. 간혹 마그네슘염만으로 저칼륨혈증이 교정되지 않을 때, 칼륨염을 투여할 수 있으며 소변의 칼륨배설을 억제시키는 spironolactone이나 amiloride 같은 알도스테론 억제제의 병용 투여가 필요하다[13]. Cha 등[14]이 고알도스테론증 소견이 동반된 20세 남자에서 spironolactone 50 mg을 단독 투여하여 저칼륨혈증 및 저마그네슘혈증이 호전되었다. Moon 등[5]이 2006년 고알도스테론증 소견은 없었던 19세 남자에서 알도스테론 길항제인 spironolactone 200 mg 투여 시에 여성형 유방의 부작용이 보고되고 있음을 고려하여 spironolactone 150 mg을 단독 투여하였으나 저칼륨혈증의 교정 경향이 없어 고알도스테론증이 없는 Gitelman 증후군 환자에서의 spironolactone 투여효과는 크지 않으며, 마그네슘의 단독 투여보다는 염화칼륨과의 복합 투여가 저칼륨혈증의 교정에 더 효과적임을 보고하였다.
본 환자에게는 염화마그네슘 및 염화칼륨과 함께 spironolactone을 4일간 투여 후 고알도스테론증 소견은 없어 spironolactone 복용은 중단하였고 혈청 칼륨 농도가 상승하고 임상증상이 호전을 보여 염화마그네슘 및 염화칼륨을 투여하면서 외래에서 추적검사한 결과 저칼륨혈증 및 저마그네슘혈증이 호전됨을 관찰할 수 있었고, 호소하는 증상도 없었다.
장기 예후는 매우 좋으며 신기능의 저하나 성장지연은 거의 없다고 알려져 있으나, 테타니 예방을 위해 일생 동안 마그네슘염의 투여가 필요하다. 본 증례와 같이 저칼륨혈증, 대사성알칼리증을 보이는 환자에게 관심을 갖는다면 Gitelman 증후군을 더 많이 진단하고 저칼륨혈증 및 저마그네슘혈증에 의한 증상을 경감시켜 좋은 예후로 이끌 수 있을 것이라 생각된다.