SMS 2012 June;18(1):26-31.
Published online 2012 July 17 |
| Copyright ⓒ 2010 Soonchunhyang Medical Science
|
| Efficacy of Intravenous Immunoglobulin Therapy in Childhood Atopic Dermatitis |
| Eun Kyeong Yeon1, A Young Park1, Sanghoon Chae1, Seung Soo Kim1, Kyeong Bae Park1, Yong Bae Kim2, Young Jin Choi3, Hae Seon Nam4, Joon Soo Park1
|
| Departments of 1Pediatrics, 2Preventive Medicine, 3Laboratory Medicine, and 4Clinical Parasitology, Soonchunhyang University College of Medicine, Cheonan, Korea |
| Corresponding Author: Joon Soo Park , Tel: +82-41-570-2163 , Fax: +82-41-572-4996 , Email: pjstable@schmc.ac.kr
|

|
ABSTRACT
|

|
|
Objective: Atopic dermatitis (AD) is a chronic inflammatory skin disease with significant morbidity, and for which there is a need for safe and effective alternative therapies. Although a few observations on the efficacy of intravenous immunoglobulin (IVIG) in AD have been reported, clinical evidence of effectiveness from controlled trials is lacking. Therefore, the purpose of this study was to clarify whether IVIG therapy (1.0 g/kg body weight at each monthly visit for 6 months) is effective in childhood atopic dermatitis and to analyze the clinical characteristics of IVIG responses in this disease.
Methods: Forty three atopic dermatitis patients who had characteristic clinical features of atopic dermatitis were included in this study. The patients received an injection of IVIG at 1.0 g/kg body weight at each monthly visit for 6 months. Laboratory tests were performed for blood chemistry, total immunoglobulin E, immunoglobulin G/immunoglobulin A/immunoglobulin M, blood eosinophil count, and C-reactive protein.
Results: In total forty three atopic dermatitis patients, only 14 patients completely underwent 6 cycles, but other 29 patients incompletely (1–5 cycles). In the 14 patients, there were just 13 records of scoring atopic dermatitis (SCORAD) index. The mean SCORAD score in the 13 patients was 39.6±24.4. SCORAD score decreased significantly (initial SCORAD, 39.6±24.4; final SCORAD, 21.3±15.6; P=0.016).
Conclusion: IVIG therapy may be recommended in the treatment of recalcitrant atopic dermatitis. In addition, further investigation on predictive markers for responses of IVIG therapy in atopic dermatitis may be needed. |
|
Keywords: Intravenous immunoglobulins; Atopic dermatitis; Child; Immunoglobulin E; Eosinophils |
|

|
서 론
|

|
|
아토피피부염은 주로 유아와 소아에 발생하는 만성 재발성 피부 염이다. 아토피피부염은 피부장벽의 손상을 초래하는 유전적 요인, 고유한 면역체계의 손상, 그리고 알레르겐과 미생물 항원에 대한 과도한 면역반응 간의 복합적인 상호관계에 의해 발생한다. 아토피 피부염에 대한 안전하고 효과적인 다양한 치료가 필요하나
[1]
, 현재 까지 아토피피부염의 근본적인 치료방법은 없는 실정으로 아토피 피부염 환자의 치료는 피부를 보호해 주는 기본적인 방법에 피부 에 대한 수분 공급과 소양감을 저하시키는 대증요법, 피부염에 대 한 치료와 유발인자의 확인 및 제거와 같은 방법들로 이루어진다
[2]
. 치료에 주로 사용되는 보습제와 항히스타민제, 국소 또는 전신 적 스테로이드를 사용하여 증상의 완화를 얻을 수 있으나 일부 환 자에서는 이러한 치료에 잘 반응하지 않는 경우도 많아 새로운 치 료에 대한 연구가 세계적으로 다양하게 이루어지고 있다
[2]
. 이러한 시점에서 정맥용 면역글로블린 치료가 임상에서 사용되 고 있으나 발열 및 두통 등 약물에 대한 부작용
[3]
이나 경제적 부담으로 인해 사용에 제한점
[4]
이 있고 아직 장기적인 효과에 대해서는 논란의 여지가 많이 남아있다. 정맥용 면역글로블린은 다양한 면역학적, 항염증성의 특성을 보인다. 고식적 치료에 반응하지 않는 아토피피부염 환자에서 정맥용 면역글로블린 치료 후 증상이 개선되었음을 증명하였다
[5]
. 정맥용 면역글로블린 치료는 가와사키, 특발성 혈소판 감소성 자반증에 효과적이나
[6,7]
, T-세포 기능과 interleukin-4 생산을 억제하는 정맥용 면역글로블린의 기능으로 아토피피부염 치료제로 이용하게 되었다
[8,9]
. 아토피피부염에서 정맥용 면역글로블린 효과에 대한 보고가 있었지만 그 효과에 대한 임상적 연구가 부족하다[10-16].
이에 본 연구에서는 정맥용 면역글로블린이 소아 아토피피부염 환자에서 효과적인지 살펴보고, 아토피피부염에 대한 정맥용 면역글로블린 효과의 예측인자에 대해 알아보고자 하였다. |

|
대상 및 방법
|

|
|
1. 대상
2008년 1월부터 2011년 6월까지 순천향대학교 천안병원 소아청소년과에서 아토피피부염으로 진단받고 경구 항히스타민제나 스테로이드연고 같은 고식적인 치료에 효과적인 반응이 없었던 환아 중 정맥용 면역글로블린을 투여하였던 43명을 대상으로 하였다. 아토피피부염의 진단은 1980년 Hanifin과 Rajka
[17]
가 제시한 진단기준을 사용하였다.
2. 방법
1) 정맥용 면역글로블린 사용
정맥용 면역글로블린(IVIG; Greencross Pharm Co, Seoul, Korea)을 1.0 g/kg로 한 달 간격으로 6회 투여하고자 하였고, 보습제, 국소적인 스테로이드 연고, 경구 항히스타민제를 병용하였다.
2) 아토피피부염의 중증도 평가
아토피피부염 환자들은 소아청소년과 의사의 문진과 시진을 통해 scoring atopic dermatitis (SCORAD) 점수에 의거하여 임상적 중증도를 평가하였다
[18]
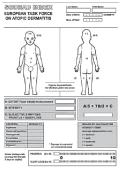
. SCORAD 평가는 병변의 범위를 9의 법칙(rule of nine)을 이용하여 두피 및 안면, 체간의 앞면 및 뒷면, 상지, 하지, 손, 음낭 부위 등을 0–100%로 측정하였다. 병변의 심한 정도는 홍반, 부종, 삼출 혹은 가피 찰상, 태선화 및 피부건조에 대하여 각각 0–3점(0=없음, 1=경도, 2=중등도, 3=중도)까지 점수를 주어 합산하였다. 주관적 증상인 소양감과 수면 장애는 최근 한 주간 심했던 정도를 0–10점(전혀 없었다=0점, 계속 있었다=10점)까지 평가하였다. SCORAD 점수의 합산(범위: 0-103)은 침범 범위(0–100)/5+침범 정도(0–18)×3.5+주관적 증상(0–20)으로 하였다
(Fig.1)
. 정맥용 면역글로블린 치료 후 SCORAD 점수가 30% 이상 감소되었을 경우에 효과가 있다고 정의하였다
[19]
.
3) 혈액검사
항원감작은 UniCAP system (Pharmacia & Upjohn, Uppsala, Sweden)을 이용하여 총 immunoglobulin E (IgE)의 정량검사를 시행하였으며 XE-2001 자동분석기(Sysmex, Kobe, Japan)를 이용하여 말초혈액 총 호산구수를 측정하였다. 그 외에도 혈청 immunoglobulin G (IgG)/immunoglobulin A (IgA)/immunoglobulin M (IgM)/IgE, 그리고 C-reactive protein (CRP)를 측정하였다.
3. 통계처리
결과는 중간값 표준편차(median standard deviation)로 표시하였고, P-value 값이 0.05 미만인 경우 의미 있는 것으로 간주하였다. 치료 후의 임상적 효과와, 치료 전후의 총 IgE, 총 호산구수, 혈청 IgG/IgA/IgM, CRP에 대한 비교는 SPSS ver. 19.0 (SPSS Inc., Chicago, IL, USA)의 Wilcoxon signed ranks test를 사용하여 통계분석하였다. |

|
결 과
|

|
|
1. 대상 환자의 특징
43명의 환자 중 14명(32.6%)만 6회의 치료를 모두 시행하였으며 나머지 29명은 6회 치료를 모두 시행하지 않았다(1–5회)
(Fig.2)
. 6회 모두 치료받은 14명 환자의 연령은 생후 15개월에서 15세까지 분포하였으며 평균 월령은 51.4개월이었고, 36개월 이하는 6명(42.9%)이었다. 남자는 6명(42.9%), 여자는 8명(57.1%)이었다
(Table 1)
. 6회 모두 치료받은 14명의 환자 중 13명만이 SCORAD 점수 기록이 남아있었다. 정맥용 면역글로블린 투여 직전에 이 13명 환자들의 평균 SCORAD 점수는 39.6±24.4점이었다.
2. 정맥용 면역글로블린 치료 전과 후의 SCORAD 점수, 소양감, 수면 장애의 변화
SCORAD 점수와 소양감 점수는 치료 전과 비교하여 정맥용 면역글로블린 치료 후 의미 있게 감소하였다. 치료 전의 SCORAD 점수는 39.6±24.4, 소양감은 6.3±3.3에서, 치료 후 각각 21.3±15.6 (P=0.016), 3.4±2.4 (P=0.013)으로 의미 있게 감소하였다(
Table 2
, Fig. 3). 수면장애의 점수는 치료 전 4.4±4.1이고, 정맥용 면역글로블린 치료 후 1.8±2.4 (P=0.050)으로 차이를 관찰할 수 없었다(
Table 2
, Fig. 3).
3. 정맥용 면역글로블린 치료 전과 후의 총 IgE, 총 호산구수, CRP, 혈청 IgG/IgA/IgM의 변화
총 IgE는 치료 전 379.2±396.3 IU/mL이고, 치료 후 436.0±632.1 IU/mL (P=0.925)로 차이를 관찰할 수 없었다(
Table 2
,
(Fig.4)
). CRP는 치료 전 1.1±2.3 mg/L이고, 치료 후 0.2±0.1 mg/L (P=0.110)으로 차이를 관찰할 수 없었다(
Table 2
,
(Fig.4)
). 총 호산구수는 치료 전 707.1±584.6/μL이고, 치료 후 350±157.6/μL (P=0.046)으로 의미 있게 감소하였다(
Table 2
,
(Fig.4)
). IgG는 치료 전 707.1±224.0 mg/dL이고, 치료 후 1,129±375.9 mg/dL (P=0.003)으로 의미 있게 증가하였다(
Table 2
,
(Fig.5)
). IgA은 치료 전 70.2±50.6 mg/dL이고, 치료 후 78.0±63.7 mg/dL (P=0.221)로 차이를 관찰할 수 없었다(
Table 2
,
(Fig.5)
). IgM은 치료 전 105.8±38.0 mg/dL이고, 치료 후 114.1±34.1 mg/dL (P=0.131)로 차이를 관찰할 수 없었다(
Table 2
,
(Fig.5)
).
4. 정맥용 면역글로블린 치료에 효과가 있었던 환자군과 효과가 없었던 환자군 비교
13명의 환자 중 정맥용 면역글로블린 치료 후 SCORAD 점수가 30% 이상 감소(효과)를 보인 환자는 7명(53.8%)이었다. 정맥용 면역글로블린 치료에 효과가 있었던 환자군에서 총 IgE, 총 호산구수, CRP, 혈청 IgG/IgA/IgM은 각각 361.8±283.7 IU/mL, 452.9±265.4 /μL, 1.7±3.4 mg/L, 745.4±251.3 mg/dL, 64.3±37.8 mg/dL, 110.5±46.6 mg/dL이고, 효과가 없었던 환자군에서는 각각 396.7±509.1 IU/mL, 961.4±720.5 /μL, 0.6±0.9 mg/L, 792.9±220.4 mg/dL, 76.1±64.1 mg/dL, 119.6±33.2 mg/dL로 두 군 간의 차이를 관찰할 수 없었다(P >0.05). |

|
고 찰
|

|
|
정맥용 면역글로불린이 아토피피부염에 효과를 미치는 기전은 몇 가지로 추측되고 있는데, 인체 내 특이 알레르겐에 대한 항체를 중화시키고 항원제시세포, 세망내피세포, B림프구의 표면에 존재하는 fragment crystallizable 수용체와 결합하여 알레르겐에 대한 자극으로 면역반응이 활성화되는 것을 차단하여 효과를 나타낸다는 가설
[3]
과 정맥용 면역글로불린자체가 T 림프구에 직접 작용하여 interleukin (IL)-4의 형성을 줄이고 T helper 2 면역반응을 억제하여 효과를 나타낸다는 가설이 있다
[8,9]
. Leung
[20]
은 정맥용 면역글로블린의 항염증성 효과가 입증되었다고 보고하였다.
1994년에 Kimata
[10]
은 정맥용 면역글로블린을 가와사키병 또는 특발성 혈소판 감소성 자반증을 동반한 아토피피부염 환자에게 처음으로 사용하였다. 최근 Gelfand 등
[11]
은 정맥용 면역글로블린은 세 명의 아토피피부염 환자에게 사용하였으며 스테로이드-의존성 아토피피부염에 효과적이라고 보고하였다. 그 외에도 몇몇에서 아토피피부염에서 정맥용 면역글로블린 효과에 대한 보고가 있었지만 그 효과에 대한 임상적 연구가 부족하다[10-16].
본 연구에서 43명의 환자 중 14명(32.6%)만 6회의 치료를 모두 시행하였으며 나머지 29명은 6회 치료를 모두 시행하지 않았다(1–5회). 6회 치료를 모두 시행하지 않은(1–5회) 29명의 환자에게 중단한 이유를 전화설문으로 조사하였다. 중단한 이유의 설문내용은 비용, 기간, 효과, 기타 등으로 중복선택이 가능하게 하였다. 29명 중 24명(82.8%)만이 답하였으며 4명은 전화연결이 되지 않았다. 전화설문에 따르면 24명 중 7명(29.2%)이 임상적 효과가 좋아서 더 이상 필요성을 못 느꼈기 때문에 중단했다고 하였다. 또한 24명 중 4명(16.7%)이 현재 6회 시행 중이라고 하였다. 그 외에도 만족도가 낮아서(4명, 16.7%), 몇 번 맞는 건지 몰라서(2명, 8.3%), 시간 맞추기가 어려워서(1명), 비싸서(1명), 병원이 멀어서(1명), 이사해서(1명), 중간에 아파서(1명), 집안 사정으로(1명) 중단했다고 조사되었다.
아토피피부염은 심한 가려움증이 동반된 만성 염증성 피부 질환으로 흔히 영유아기에 발현한다. 전 세계적으로 약 10–30%의 인구가 아토피피부염을 가지고 있으며, 우리나라에서도 최근 환자가 급격히 증가하는 추세에 있다. Lee 등
[21]
은 소아 아토피피부염이 1세 미만이 18예(20%), 1–3세가 32예(35.6%), 4–6세가 20예(22.2%), 7세 이상이 20예(22.2%)이었다고 하였다. 나이 분포는 생후 3개월에서 18세까지로 다양하였으며, 성별로는 남자 50예, 여자 40예로 남자가 많았다고 하였다. 이번 연구에서는 6회 모두 치료받은 14명 환자의 연령은 생후 15개월에서 15세까지 분포하였으며 평균 월령은 51.4개월이었고, 36개월 이하는 6명(42.9%)이었고 36개월 이상은 8명(57.1%)이었다. 남자는 6명(42.9%), 여자는 8명(57.1%)으로 남녀 비는 1:1.3이었다. 이번 연구에서는 36개월 미만군이 36개월 이상군보다 많아서 Lee 등
[21]
의 논문과의 차이를 보이는데, 이것은 본 연구가 고식적인 치료에 효과적인 반응이 없었던 환아를 대상으로 하였기 때문에 차이가 나는 것으로 생각된다.
6회의 정맥용 면역글로블린을 투여받은 13명의 환자 중 정맥용 면역글로블린 치료 후 SCORAD 점수가 30% 이상 감소(효과)를 보인 환자는 7명(53.8%)이었고, 조금이라도 감소를 보인 환자는 11명(84.6%)이었다. 즉, 치료 전의 SCORAD 점수는 39.6±24.4, 소양감은 6.3±3.3에서, 치료 후 각각 21.3±15.6 (P=0.016), 3.4±2.4 (P=0.013)으로 감소하였다(
Table 2
, Fig. 3).
결과적으로, 53.8% 환자가 SCORAD 점수가 30% 이상 감소하였으며 84.6% 환자가 SCORAD 점수가 조금이라도 감소를 보였으며, SCORAD 점수와 소양감은 치료 전과 비교하여 정맥용 면역글로블린 치료 후 의미 있게 감소하였다. 이러한 결과는 정맥용 면역글로블린이 아토피피부염에서 비교적 임상적인 효과가 있음을 시사한다.
그러나 수면장애는 치료 전과 비교하여 치료 후 감소하였지만 통계학적인 의미를 관찰할 수 없었다(
Table 2
, Fig. 3). 따라서 수면장애에서 정맥용 면역글로블린의 효과에 대한 연구가 더 필요하다.
본 연구에서는 총 IgE는 치료 전후 차이를 관찰할 수 없었다(
Table 2
,
(Fig.4)
). Abemathy 등
[22]
이 발표한 연구에 따르면 일반적으로 아토피피부염 환자에게 정맥용 면역글로블린 치료 후에 상승했던 IgE가 현저하게 감소된다고 알려져 있으며, Gelfand 등
[11]
은 치료 후에 IgE의 감소가 있지만 현저하지는 않다고 보고하고 있다. 이렇게 아직까지 정맥용 면역글로블린 치료와 혈청 IgE치와의 상관관계에 대해서는 논란이 있는 상태이므로 총 IgE 변화가 아토피피부염 경과에 직접적인 영향을 주지 않는 것인지에 관하여 더 많은 연구가 요구된다.
본 연구에서는 총 호산구수는 치료 전과 비교하여 치료 후 의미 있게 감소하였다(
Table 2
,
(Fig.4)
). 아토피피부염에서는 말초혈액 내 호산구수의 증가를 볼 수 있는 것으로 보고되고 있으며
[23]
호산구증가증은 임상적 중증도와 상관관계가 있다고 알려져 있다
[24]
. Kimata
[10]
은 호산구증가증이 임상적 반응과 관련되어 있고 정맥용 면역글로블린 치료 후에 호산구가 효과적으로 감소하였다던 보고와 유사한 결과를 보였다.
본 연구에서는 염증반응의 지표로 CRP를 사용하였으며, 치료 전과 비교하여 정맥용 면역글로블린 치료 후 차이를 관찰할 수 없었다(
Table 2
,
(Fig.4)
). 일반적으로 soluble IL-2 receptor (sIL-2R), intercellular adhesion moleeule-1 (ICAM-1), endothelial leukocyte adhesion molecule (ELAM-1), eosinophil cationie protein (ECP) 등을 아토피피부염의 염증반응의 지표로 이용하고 있다[25-27]. Jee 등
[28]
은 정맥용 면역글로블린 치료 후에 ICAM-1, ECP가 의미 있게 감소하였으며, ICAM-1, ECP가 정맥용 면역글로블린의 염증반응 지표로 효과적이라고 보고하였다. 그러나 Halmerbauer 등
[25]
은 아토피피부염 치료 후에 SCORAD score의 변화와 비교했을 때 sIL-2R와 ECP가 유의한 차이를 보이나, ICAM-1 또는 ELAM-1는 차이를 관찰할 수 없다고 보고하고 있어 아토피피부염의 염증반응의 지표에 대해서는 아직 논란의 여지가 있다. 따라서 향후 정맥용 면역글로블린의 항염증성 효과를 반영하는 유용한 지표에 대한 지속적인 연구가 필요할 것이다.
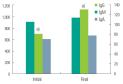
본 연구에서는 IgG는 치료 전과 비교하여 치료 후 의미 있게 증가하였다(
Table 2
,
(Fig.5)
). 그러나 IgA와 IgM은 치료 전후 차이를 관찰할 수 없었다(
Table 2
,
(Fig.5)
). Varelzidis 등
[29]
의 연구에서는 아토피피부염에서 IgG와 IgA가 의미 있게 증가하고, IgM은 변화가 없었으며 Fraser 등
[30]
의 연구에서는 IgA는 의미 있게 증가하였으나 IgG 증가와 IgM 감소는 유의하지 않다고 보고하였고, Lai와 van Furth
[31]
의 연구에서는 IgM만이 의미 있게 감소하고, IgG 감소와 IgA 증가는 유의하지 않다고 하였다. 아토피 질환에서 IgE의 증가가 있었으나 IgG, IgA, IgM와 아토피 질환과 관련 없다는 보고도 있었다
[32]
. 그러나 본 연구에서 IgG값의 상승은 정맥용 면역글로블린 투여에 따른 현상으로 해석할 수 있겠다. 그러나 치료군에서 치료 전 IgG값이 정상군의 값에 비해 상대적으로 낮은 군에서 이러한 효과를 보인 것은 아닌지에 대하여 좀 더 연구가 필요하다고 생각된다.
본 연구에서는 정맥용 면역글로블린 사용 적응증을 알아보고자 SCORAD 점수 30% 이상 감소를 보였던 환자군과 30% 미만 감소를 보인 환자군의 각각의 IgE, 총 호산구수, CRP, IgG, IgA, IgM의 평균을 비교하였다. 치료에 효과가 있었던 환자군에서 총 IgE, 총 호산구수, CRP, 혈청 IgG/IgA/IgM은 각각 361.8±283.7 IU/mL, 452.9±265.4/μL, 1.7±3.4 mg/L, 745.4±251.3 mg/dL, 64.3±37.8 mg/dL, 110.5±46.6 mg/dL이고, 효과가 없었던 환자군에서는 각각 396.7±509.1 IU/mL, 961.4±720.5/μL, 0.6±0.9 mg/L, 792.9±220.4 mg/dL, 76.1±64.1 mg/dL, 119.6±33.2 mg/dL이었다. 결과적으로 이번 연구에서는 두 군 간의 차이를 관찰할 수 없었다(P>0.05). 따라서 어떤 군에서 정맥용 면역글로블린을 투여하면 효과가 있을지에 관한 결과는 얻을 수 없었다. 한편, 정맥용 면역글로블린과 면역학적 및 항염증성 변화와는 직접적인 상관관계를 보이지 않아, 증상의 변화가 면역학적 및 항염증성 변화와 반드시 일치하지 않음을 알 수 있었다. 이는 아마도 말초혈액에서의 변화만 관찰할 수 밖에 없었던 연구의 제한점으로 생각할 수 있으며, 또한 SCORAD 점수는 증상을 주관적으로 측정하는 것으로서 환자 개인에 따른 여러 다른 요인이 관련될 수 있어 이러한 결과를 초래하였을 가능성이 있다.
결론적으로 정맥용 면역글로블린 치료는 아토피피부염에서 임상적인 효과적일 수 있음을 확인할 수 있었다. 향후 아토피피부염에 대한 정맥용 면역글로블린 효과의 예측인자에 대한 체계적인 연구가 지속되어야 할 것이다. |
|

|
FIGURES
|

|
|
|
Fig.1
Scoring atopic dermatitis (SCORAD) index. |

|

|
Fig.2
Participant flow. SCORAD, scoring atopic dermatitis. |

|

|
Fig.3
Scoring atopic dermatitis (SCORAD) index, sleep loss, prutitus score at initial and final intravenous immunoglobulin treatment. SCORAD index and pruritus score decreased significantly. But, sleep loss score did not change significantly.a)SCORAD, P=0.016. b)Prutitus, P=0.013. |

|

|
Fig.4
Immunoglobulin E (IgE), eosinophilic counts, C-reactive protein (CRP) at initial and final intravenous immunoglobulin treatment. Eosinophilic counts decreased significantly. But, IgE and CRP did not change significantly. a)Eosinophilic count, P=0.046. |

|
|
Fig.5
Immunoglobulin G (IgG), immunoglobulin A (Iga), immunoglobulin M (IgM) at initial and final intravenous immunoglobulin treatment. IgG increased significantly. But, IgM and IgA did not change significantly. a)IgG P=0.003. |

|
|

|
TABLES
|

|
|

|
Table.1
Baseline characteristics of patients |

|

|
Table.2
Comparison of SCORAD index, serum IgE, eosinophil counts, CRP, IgG/IgA/IgM at initial and final IVIG treatment |

|
|
| |

|
REFERENCE
|

|
|
|
1.
|
Graham-Brown RA. Therapeutics in atopic dermatitis. Adv Dermatol 1997;13:3-3 |
|
2.
|
Lee JH, Kim KH, Kim MN, Kim JW, Ro YS, Park YL, et al. Report from ADRG: the treatment guideline of Korean atopic dermatitis. Korean J Dermatol 2006;44:907-13. |
|
3.
|
Duhem C, Dicato MA, Ries F. Side-effects of intravenous immune globulins. Clin Exp Immunol 1994;97 Suppl 1:79-8 |
|
4.
|
Jolles S, Sewell C, Webster D, Ryan A, Heelan B, Waite A, et al. Adjunctive high-dose intravenous immunoglobulin treatment for resistant atopic dermatitis: efficacy and effects on intracellular cytokine levels and CD4 counts. Acta Derm Venereol 2003;83:433-7. |
|
5.
|
Rabinovitch N, Gelfand EW, Leung DY. The role of immunoglobulin therapy in allergic diseases. Allergy 1999;54:662-8. |
|
6.
|
Furusho K, Kamiya T, Nakano H, Kiyosawa N, Shinomiya K, Hayashidera T, et al. High-dose intravenous gammaglobulin for Kawasaki disease. Lancet 1984;2:1055-8. |
|
7.
|
Imbach P, Barandun S, d’Apuzzo V, Baumgartner C, Hirt A, Morell A, et al. High-dose intravenous gammaglobulin for idiopathic thrombocytopenic purpura in childhood. Lancet 1981;1:1228-31. |
|
8.
|
Leung DY. Atopic dermatitis: immunobiology and treatment with immune modulators. Clin Exp Immunol 1997;107 Suppl 1:25-30. |
|
9.
|
Jolles S, Hughes J, Rustin M. Intracellular interleukin-4 profiles during high-dose intravenous immunoglobulin treatment of therapy-resistant atopic dermatitis. J Am Acad Dermatol 1999;40:121-3. |
|
10.
|
Kimata H. High dose gammaglobulin treatment for atopic dermatitis. Arch Dis Child 1994;70:335-6. |
|
11.
|
Gelfand EW, Landwehr LP, Esterl B, Mazer B. Intravenous immune globulin: an alternative therapy in steroid-dependent allergic diseases. Clin Exp Immunol 1996;104 Suppl 1:61-6. |
|
12.
|
Jolles S, Hughes J, Rustin M. The treatment of atopic dermatitis with adjunctive high-dose intravenous immunoglobulin: a report of three patients and review of the literature. Br J Dermatol 2000;142:551-4. |
|
13.
|
Huang JL, Lee WY, Chen LC, Kuo ML, Hsieh KH. Changes of serum levels of interleukin-2, intercellular adhesion molecule-1, endothelial leukocyte adhesion molecule-1 and Th1 and Th2 cell in severe atopic dermatitis after intravenous immunoglobulin therapy. Ann Allergy Asthma Immunol 2000;84:345-52. |
|
14.
|
Wakim M, Alazard M, Yajima A, Speights D, Saxon A, Stiehm ER. High dose intravenous immunoglobulin in atopic dermatitis and hyper-IgE syndrome. Ann Allergy Asthma Immunol 1998;81:153-8. |
|
15.
|
Kimata H. High-dose intravenous gamma-globulin treatment for hyperimmunoglobulinemia E syndrome. J Allergy Clin Immunol 1995;95:771-4. |
|
16.
|
Noh G, Lee KY. Intravenous immune globulin (i.v.IG) therapy in steroid-resistant atopic dermatitis. J Korean Med Sci 1999;14:63-8. |
|
17.
|
Hanifin JM, Rajka G. Diagnostic features of atopic dermatitis. Acta Derm Venereol (Stockh) 1980;Suppl 92:44-7. |
|
18.
|
European Task Force on Atopic Dermatitis. Severity scoring of atopic dermatitis: the SCORAD index. Consensus Report of the European Task Force on Atopic Dermatitis. Dermatology 1993;186:23-31. |
|
19.
|
Nahm DH, Lee ES, Park HJ, Kim HA, Choi GS, Jeon SY. Treatment of atopic dermatitis with a combination of allergen-specific immunotherapy and a histamine-immunoglobulin complex. Int Arch Allergy Immunol 2008;146:235-40. |
|
20.
|
Leung DY. The immunologic effects of IVIG in Kawasaki disease. Int Rev Immunol 1989;5:197-202. |
|
21.
|
Lee HS, Kim JS, Pyun BY. Changes of the prevalence and the allergens of atopic dermatitis in children: in between the year of 1992 and 2002. Pediatr Allergy Respir Dis 2002;12:263-71. |
|
22.
|
Abernathy RS, Strem EL, Good RA. Chronic asthma in childhood: double-blind controlled study of treatment with gamma-globulin. Pediatrics 1958;21:980-93. |
|
23.
|
Weller PF. Eosinophilia. J Allergy Clin Immunol 1984;73(1 Pt 1):1-14. |
|
24.
|
Walker C, Kägi MK, Ingold P, Braun P, Blaser K, Bruijnzeel-Koomen CA, et al. Atopic dermatitis: correlation of peripheral blood T cell activation, eosinophilia and serum factors with clinical severity. Clin Exp Allergy 1993;23:145-53. |
|
25.
|
Halmerbauer G, Frischer T, Koller DY. Monitoring of disease activity by measurement of inflammatory markers in atopic dermatitis in childhood. Allergy 1997;52:765-9. |
|
26.
|
Kowalzick L, Kleinheinz A, Neuber K, Weichenthal M, Köhler I, Ring J. Elevated serum levels of soluble adhesion molecules ICAM-1 and ELAM-1 in patients with severe atopic eczema and influence of UVA1 treatment. Dermatology 1995;190:14-8. |
|
27.
|
Wakita H, Sakamoto T, Tokura Y, Takigawa M. E-selectin and vascular cell adhesion molecule-1 as critical adhesion molecules for infiltration of T lymphocytes and eosinophils in atopic dermatitis. J Cutan Pathol 1994; 21:33-9. |
|
28.
|
Jee SJ, Kim JH, Baek HS, Lee HB, Oh JW. Long-term Efficacy of Intravenous Immunoglobulin Therapy for Moderate to Severe Childhood Atopic Dermatitis. Allergy Asthma Immunol Res 2011;3:89-95. |
|
29.
|
Varelzidis A, Wilson AB, Meara RH, Turk JL. Immunoglobulin levels in atopic eczema. Br Med J 1966;2:925-7. |
|
30.
|
Fraser NG, Dick HM, Crichton WB. Immunoglobulins in dermatitis herpetiformis and various other skin diseases. Br J Dermatol 1969;81:89-95. |
|
31.
|
Lai A Fat RF, van Furth R. Serum immunoglobulin levels in various skin diseases. Clin Exp Immunol 1974;17:129-37. |
|
32.
|
Orgel HA, Lenoir MA, Bazaral M. Serum IgG, IgA, IgM, and IgE levels and allergy in Filipino children in the United States. J Allergy Clin Immunol 1974;53:213-22. |
|
|
|