서 론
근이영양증(myotonic dystrophies, DM)은 골격근의 점진적인 악화와 퇴행을 특징으로 하는 이질성의 유전장애 질환군이다[1]. 근이영양증의 증상은 골격근뿐만 아니라 심장, 폐와 같은 중요 장기들에도 직접적인 영향을 미친다. 이로 인해 근이영양증 환자들의 전신마취 시에 심부정맥, 빈번한 빈맥과 같은 심혈관계 합병증뿐만 아니라 호흡중추의 억제로 인한 중심성 무호흡증과 자발호흡으로의 전환 지연과 같은 호흡기적 합병증이 발생할 수 있다[1-3]. 특히 근이영양증 환자의 근이완 회복 시에 항콜린에스터라제의 사용은 잔류 근이완효과의 연장이나 근긴장증을 유발하여 환자의 마취에서의 회복 지연이 보고되고 있다[1,4]. 수술 후 근이영양증 환자는 호흡근의 이완으로 인해 폐 합병증 발생비율이 높고, 이로 인하여 중환자실 입원 및 사망에 이르는 경우도 보고되고 있다[4-6]. 최근 여러 연구에서는 sugammadex를 이용하여 위와 같은 호흡기계의 문제없이 환자를 성공적으로 각성시키는 사례들이 보고되고 있다[4]. 저자들 또한 근이영양증 환자에게서 완전정맥마취(total intravenous anesthesia, TIVA)를 시행하고 Sugammedex를 사용하여 성공적으로 전신마취를 시행하였기에 이를 보고하고자 한다.
증 례
이 증례보고는 출판을 위해 입원 당시 환자로부터 의학정보의 연구자료 이용 동의를 얻었다. 환자는 33세 남성으로 왼쪽 겨드랑이에 화농성 한선염(hidradenitis suppurativa)을 진단받고 이에 대한 절제생검과 반흔구축성형술을 위해 입원하였다. 환자는 2005년에 유전자검사를 통해 비정상적인 근이영양증 kinase 유전자 내에 비정상적인 CTG (cytosine-thymine-guanine) 반복서열을 확인함으로써 1형 근이영양증을 진단받았다. 환자는 양손으로 물건을 쥘 때 힘이 빠지는 증상을 호소하였으며, 심부건 반사검사에서 양쪽 발목 인대 반사의 유의미한 감소를 보였다. 근전도검사에서는 우측 짧은엄지벌린근(abductor pollicis brevis)과 우측 앞정강근(tibialis anterior muscles)에서 중증의 근긴장성 전위(myotonic discharges)가 발견되었다. 위의 결과를 종합하였을 때, 원위부 사지에서의 반복적인 근긴장증과 간헐적 근력 약화가 있는 것을 확인할 수 있었다. 얼굴에서는 혀의 타진근경직증(percussion myotonia) 소견을 보이고 있었으나, 그 이외에 연하곤란, 구음장애, 안검하수, 백내장 등의 소견은 보이지 않아 muscular impairment rating scale grade III로 판정되었다[5] (Table 1). 이전에 수면장애를 진단받거나 폐 흡인으로 인한 입원력은 없었으며 부정맥과 같은 심장의 이상소견은 보이지 않았다.
가족력상 큰 누나와 고모가 양손의 간헐적 근긴장증과 근력악화 증상이 있었으나 근이영양증으로 진단받지는 않았다. 그 외의 기저질환으로 당뇨를 2010년 진단받았으며 metformin과 linagliptin을 복용 중이었다. 환자는 세팔로스포린계 항생제에 대해 전신 소양증과 가려움증을 주소로 한 알러지반응 과거력이 있었다.
수술 전 검사에서 환자의 키와 몸무게는 169.2 cm에 76.8 kg이었다. 심전도검사에서 심박수는 분당 116회의 동성 빈맥 소견이 보였으며, 심초음파상 좌심실 박출률은 62%, 좌심실 충만기의 비정상적 확장패턴 이외의 특이소견은 관찰되지 않았다. 폐기능검사에서 1초호기노력량(forced expiratory volume at 1 second, FEV1) 4.44 L (89%), 노력폐활량(forced vital capacity, FVC) 4.74 L (92%), FEV1/FVC ratio 93.6%로 정상 폐기능 소견을 보였으며, 호흡 시 보조호흡근의 사용 없이 호흡하고 있음을 확인하였다. 입을 최대로 벌렸을 때 치아 사이 간격은 6.5 cm였고, Mallampati class II 소견을 보였다. 시행한 혈액검사에서 당화혈색소 7.8% 이외의 특이소견은 없었다. 측정된 혈압은 120/70 mm Hg, 호흡수는 18회였다.
환자의 마취방법으로는 TIVA를 이용한 전신마취를 시행하기로 하였다. 환자는 오른팔에 18 게이지 정맥주사라인을 거치하고 수술방에 입실하였다. 심전도, 비침습적 혈압계, 산소포화도 측정 장치를 거치하고, 마취심도를 확인하기 위해 bispectral index를, 환자의 수술 중 근이완정도를 감시하기 위해 사연속자극(train of four, TOF) 장치를 환자의 오른쪽 짧은엄지벌린근에 부착하였다. 마취 시작 전 혈압은 132/68 mm Hg, 심박수는 분당 103회로 측정되었고, 심전도상 동성 빈맥이 관측되었다. Target controlled infusion을 이용하여 propofol 5 μg/mL와 remifentanil 3 ng/mL로 마취 유도를 시작하였으며, 근이완제로는 rocuronium 30 mg을 사용하였다. 마취 유도 직전 측정된 TOF ratio는 99%였으며, 45초 후 TOF ratio가 0%가 된 것을 확인하였고, 근이완제 주입 후 1분 뒤에 윤상연골 압박을 시행하며 기관삽관을 시행하였다.
수술시간은 총 35분 소요되었으며, 수술 중 propofol 4 μg/mL와 remifentanil 1 ng/mL로 마취를 유지하였다. 수술 중 지속적으로 감시한 TOF ratio는 0%였으며, 추가적으로 투여한 근이완제는 없었다. 수술 중 심전도에서 부정맥 소견은 보이지 않았으며, 저혈압은 발생하지 않았다. 수술 종료 후 근이완 역전을 위해 sugammadex 200 mg을 주입하였다. Sugammadex 주입 시점에서 TOF ratio는 0%, 1분 후 TOF ratio 75%, 2분 후 TOF ratio 93%, 3분 이후에는 TOF ratio 99% 이상이 측정되었다. Sugammadex 주입 후 8분 후부터 환자의 자발호흡이 가능해졌으며, sugammadex 주입 10분 후 환자가 눈을 뜰 수 있었고, sugammadex 주입 12분 후 환자는 스스로 목을 가누어 올릴 수 있었고, 호흡 수도 분당 16회, 1회 호흡량 6 mL/kg 이상이 유지됨을 확인하여 발관을 시행하였다.
환자는 즉시 회복실로 옮겨졌으며, 이 곳에서 단순 마스크로 5 L/min의 산소를 공급받으며, 심전도, 비침습적 혈압, 산소포화도를 감시하였다. 30분 동안의 회복실 체류기간에 환자는 잦은 기침, 호흡근의 불규칙한 움직임, 호흡곤란, 삼킴곤란 등의 근긴장 및 호흡기계 증상은 발생하지 않았다. 환자는 명확히 자기 이름을 말하고 원활하게 의사소통이 가능했으며 의식은 명료하였다. 환자의 산소포화도는 단순 마스크 제거 후에도 99% 미만으로 감소하지 않아 병실로 이송되었다.
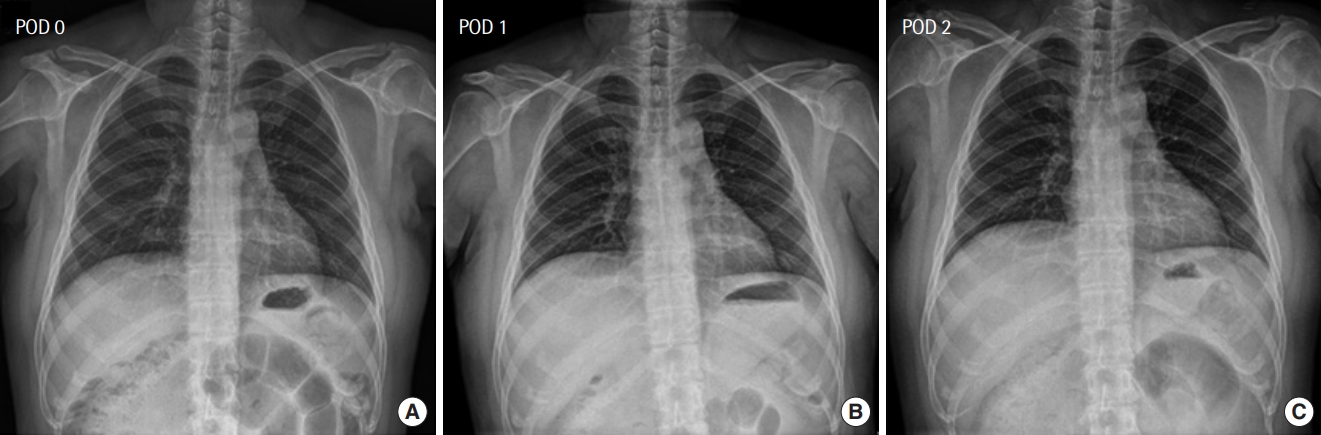
수술 당일 환자의 호흡기 증상은 보이지 않았으며, 시행한 흉부 방사선검사에서 폐 음영의 증가나 무기폐의 소견은 관찰되지 않았다. 수술 후 1일째, 2일째 모두 호흡기계 증상은 없었으며, 시행한 흉부 방사선검사에서 폐 음영의 증가나 무기폐의 소견은 관찰되지 않았다(Fig. 1). 환자는 수술 후 2일째에 특이증상 호소 없이 정상 퇴원하였다.
고 찰
근이영양증은 골격근에 대한 영향뿐만 아니라 중추신경계, 심장, 폐, 내분비, 소화기관에 모두 직접적으로 작용하는 근육이상 유전질환 중 하나이다. 유병률은 전 세계적으로 신생아 중 8,000명당 1명이며, 전 세계 인구 10만 명당 2–14명 정도로 알려져 있다[1,7]. 근이영양증은 제1형과 제2형의 두가지 타입으로 나뉘며, 제1형 근이영양증(Steinert disease)은 신생아부터 성인까지 모든 연령대에서 발생할 수 있고, 반면 제2형 근이영양증(proximal myotonic myopathy)은 성인에게서만 발생하며, 증상의 중증도는 제1형에서 심한 것으로 알려져 있다[1,3].
제1형 근이영양증은 다시 그 발병시기에 따라 선천성(congenital), 청소년기 발현성(childhood-onset), 성인기 발현성(adult-onset)으로 나뉜다. 그 중 성인기 발현성 제1형 근이영양증이 가장 흔하며, 15세에서 35세 사이에 그 증상이 처음 나타나게 된다[1]. 임상 양상으로는 악수를 하는 것을 어려워하고, 말을 하거나 씹을 때 사용하는 구근육(bulbar muscle)의 약화로 삼키거나 말하는데 문제가 있다. 또한 안검하수를 동반한 양측 얼굴의 근력 약화와 앞머리 탈모와 같은 전형적인 “근긴장성 얼굴(myotonic facies)”이 나타날 수 있다[1,2]. 본 증례에서 환자는 18세에 양 손에 힘이 빠지는 증상을 주소로 진단받은 성인기 발현성 제1형 근이영양증이며, 혀의 타진근경직증은 있었으나 구근육의 약화 소견은 없어 삼킴장애나 구음장애가 나타나지 않았으며, 외적으로도 전형적인 근긴장성 얼굴의 형태를 하지 않은 점이 특징적이었다.
근이영양증의 심장이상은 심장근육세포의 미토콘드리아에 조밀한 과립이 생성되고, 이 과립이 심장세포의 괴사, 지방 침윤 및 섬유증을 초래하여 심장전도시스템의 과흥분성을 유발하여 발생한다[7]. 이로 인하여 자주 두근거리는 증상과 더불어 고혈압, 심부전, 심비대가 나타나게 되고, 심실성 부정맥이 발생할 확률이 증가하게 된다. 심전도 소견으로 좌심실 비대, 방실 차단, 좌각 완전 차단, 양속 차단, 심실 세동 등이 관찰된다. 이러한 심전도의 소견은 제1형 근이영양증 환자에서 급사(sudden cardiac death)의 위험요소를 평가하는 기준이며, 심질환이 근이영양증 환자에서 가장 흔한 사망원인이 되게 한다[5,7]. 본 증례에서는 환자가 이전에 진단받은 심장질환이나 심기능의 이상은 없었으며, 수술 전 심전도검사에서 동성 빈맥 소견만 있었고, 심초음파검사에서 정상 좌심실 박출률과 심근의 이상소견은 관찰되지 않아, 수술 중후 심혈관계 합병증의 발생 가능성이 다른 환자들에 비해서 낮을 수 있음을 확인할 수 있었다.
근이영양증의 호흡기계 이상은 증상 발생 초기에 상기도와 호기근 및 횡격막의 근육 약화와 근긴장에 의해 발생한다[6,8]. 상기도 근육의 경우 중추신경의 호흡조절 중추 또한 근이영양증의 영향을 받게 되어 기능저하가 나타나게 되고, 이로 인해 폐쇄성 무호흡, 폐흡인의 증상이 나타나게 된다. 호기근의 약화는 환자로 하여금 적절한 기침을 할 수 없게 만들고, 그로 인해 무기폐가 나타날 수 있다[6]. 위와 같은 원인들로 인하여 폐포 저환기(alveolar hypoventilation), 만성 과탄산증과 더불어 FEV1, FVC, 총 폐활량(total lung capacity)이 모두 감소된 제한성 폐기능 장애소견을 보이게 된다[8]. 본 증례에서는 폐기능검사상 FVC, FEV1 정상소견을 보였으며, 수면무호흡증이나 폐 흡인으로 인한 입원력은 없는 것으로, 호흡기계 침범이 심하지 않았다.
근이영양증 환자의 호흡기계 문제는 전신마취에서 회복 시에 더 문제가 된다. 환자의 구근육과 호흡근의 약화로 인하여 환자가 자발호흡회복의 지연이 보고되고 있다[1]. 특히 neostigmine과 같은 항콜린에스터라제를 사용하는 경우 오히려 환자의 호흡근의 수축을 증가시키거나 호흡근의 마비를 악화시킨다는 보고가 있어서 신중히 사용하여야 한다[2,9]. 한편, sugammadex는 개량된 γ‐cyclodextrin 제재로, rocuronium 혹은 vecuronium과 1 대 1로 직접 결합하여 근이완을 역전시켜 잔류 근이완을 줄여줄 뿐만 아니라 아세틸콜린에스터라제를 억제하지 않는다[4,10]. 이러한 장점으로 인해 근이영양증이 있는 환자들의 전신마취에서 성공적으로 사용이 보고되었다[4]. 2018년의 Ahmed 등[4]의 연구에서 근이영양증으로 진단받은 성인에게 전신마취를 시행한 6개의 증례보고에서 전신마취를 실시한 성인 환자들의 최소 sugammadex 사용 용량은 2 mg/kg이고, TOF 비가 0.9 이상에 도달하기까지 걸린 가장 짧은 시간은 30초였으며, 나머지 5개 증례에서 모두 2분 이내에 TOF 비가 0.9 이상에 도달하였고, 잔류 근이완이나 근육이완재현(recurarization)은 모든 증례에서 발생하지 않았다고 보고하였다. 본 증례에서는 sugammadex 200 mg을 사용하여 2 mg/kg보다 더 많은 용량을 사용하였고, TOF 비가 0.9 이상에 도달하기까지 2분이 걸렸으므로, 상기 증례들의 결과와 부합하는 소견을 보인다. 하지만 수술방에서 발관 시 발관시간에 대해 명확히 언급한 증례는 없었기에 이에 대한 비교는 어려웠다.
근이영양증 환자의 호흡기계적 문제는 수술 후 호흡기계 합병증과도 연관이 있다. 근이영양증 환자의 수술 후 합병증에서 폐 합병증이 가장 많은 요인을 차지하였으며, 이는 근이영양증 2형보다 1형에서 더 두드러지게 나타났다[3,6]. 폐 합병증의 증상과 원인으로는 호흡근의 약화로 인하여 무기폐가 잘 생기며, 인두근육의 약화로 인하여 폐 흡인의 문제가 나타날 수 있고, 호흡중추의 저하 문제는 환자의 폐포 저환기를 악화시키고, 급성 호흡곤란을 유발할 수도 있다[6]. 한편, Ahmed 등[4]의 연구에서 근이영양증을 진단받은 6명의 성인 환자에게 sugammadex를 사용한 모든 증례에서 수술 후 폐 합병증이 발생하지 않았다고 보고하였다. 위의 증례 중 한 명은 수술 후 기계 환기를 시행하여 수술 종료 후 2시간 30분 이후 자발호흡을 확인하고 발관을 시행하였는데, 이 환자의 경우에도 폐합병증의 증상을 호소하지 않았다고 보고하였다. 본 증례의 환자에서도 수술 후 회복실에서 자발호흡을 잘 유지하였으며, 퇴원 전까지 폐흡인이나 발열 등의 소견이 없었고 단순 흉부 X선 촬영에서도 무기폐와 같은 소견 없이 정상소견을 유지하였다. 따라서 근이영양증 환자의 전신마취에서 sugammadex의 사용은 각성 시의 지연을 줄여주고 안전하게 환자를 각성시킬 수 있을 뿐 아니라 근이영양증 환자에게서 가장 흔하게 발생하는 폐 합병증을 줄여줄 수 있을 것이라고 예측해 볼 수 있으나, 이에 대하여서는 전신마취를 받는 근이영양증 환자들의 수술 후 재원기간의 합병증을 비교해보는 추가연구가 더 필요할 것으로 보인다.
결론적으로, 본 저자들은 말단부 근이상 소견을 보이며, 직접적인 심폐기능의 침범은 없는 제1형 근이영양증 환자에서의 전신마취에서 TIVA를 사행하고, 각성 시 sugammadex를 사용하여 호흡기계 합병증 없이 성공적으로 마취회복을 시행하여 이를 보고하는 바이다.